于政权课题组最新研究发现炎症性肠病新的治疗靶点
本网讯 3月4日,国际知名学术期刊The EMBO Journal在线发表了我校生物学院于政权教授课题组最新研究成果。该成果揭示了间充质微环境信号激活肠上皮损伤修复的分子机制,为治疗炎症性肠病发现重要治疗靶点。
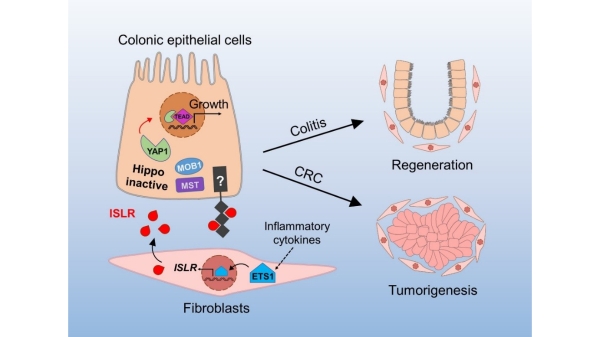
于政权介绍说,炎症性肠病(IBD)是一类病因不明确和难以治愈的慢性肠道炎症性疾病,主要包括溃疡性结肠炎和克罗恩病。近年来,IBD的发病率在我国迅速增长,且患者年龄呈现年轻化的趋势,已经成为影响我国人民健康的重要难题。IBD主要表现为肠道慢性炎症和肠道屏障功能受损。因此,揭示肠上皮损伤修复的分子调控机制不仅有助于深入认识IBD的致病和恢复机理,也将为临床药物设计和疾病防治提供重要的科学依据和新的靶点。
我校生物学院的博士生徐久智解释说,“在肠道组织损伤修复过程中,上皮细胞中多个信号通路相互协调,共同发挥调控作用。其中,进化上高度保守的Hippo信号通路对于细胞增殖和组织再生必不可少。在正常生理情况下,Hippo信号处于激活状态,而YAP作为其下游的关键转录激活因子,则处于相对抑制的状态,从而限制肠上皮细胞过度增殖,防止组织增生及肿瘤发生。相反,在炎症引起的肠上皮损伤修复过程中,Hippo信号通路被抑制,而YAP被激活以促进组织再生。然而,在肠道炎症反应中,通过何种方式控制Hippo信号通路来启动上皮再生的调控机制仍尚未明确”。
已有研究表明间充质微环境在上皮组织损伤修复中发挥极为重要的功能。在本研究中,他们发现炎症信号在微环境的间充质细胞中诱导表达的转录因子ETS1,能够直接调控间充质细胞表达一种分泌型的ISLR蛋白;分泌到细胞外的ISLR蛋白通过结合到肠上皮细胞表面的特定膜蛋白来抑制上皮细胞内Hippo信号通路,激活YAP,进而加快上皮细胞增殖,促进肠上皮组织修复。在小鼠肠道间质细胞中特异性敲除ISLR之后,小鼠肠道上皮的组织损伤后再生修复能力显著下降。同时还发现,敲除ISLR可以显著抑制小鼠肠癌的发生发展,而ISLR在结直肠癌病人中的表达水平与肿瘤恶性程度及不良预后高度正相关。以上结果表明间充质细胞分泌的ISLR通过抑制肠上皮细胞的Hippo信号通路来激活上皮再生过程。
于政权表示,本研究成果揭示了炎症信号启动上皮再生过程的“开关”。通过控制ISLR的水平可以调控肠上皮的损伤修复程序。然而,过度并持续的提高ISLR水平则可能诱发肿瘤发生。因此,ISLR具有作为治疗IBD和结直肠癌药物靶点的潜力。近年来,肿瘤微环境作为肿瘤治疗的重要靶点,已经取得了重大成功。相信肠道炎症的微环境也同样有可能作为治疗炎症性肠病的重要靶点。“接下来,我们将从炎症微环境的角度探索炎症性肠病新的治疗靶点和策略”,于政权说。
我校生物学院博士生徐久智和中科院生化细胞所的汤扬博士后为共同第一作者;分子细胞科学卓越创新中心/生化与细胞所的周兆才研究员为该论文的共同通讯作者;中国农业大学生物学院孟庆勇课题组提供了Islr条件性敲除小鼠。
